Glikokortikoidi
Glikokortikoidi se sintetiušu u zoni fasciculati, imaju 21 karbonsku strukturu i označavaju se kao 17-hidroksikortikosteroidi ili kortikosteroidi. Glavni glikokortikoid je kortizol koji se u perifernim tkivima pretvara u kortizon uz pomoć enzima 11ß hidroksisteroid dehidrogenaze. Najmanje 95% od ukupne glikokortikoidne djelatnosti hormona koji se luče iz kore nadbubrežnih žlijezda, otpada na kortizol. Kortizol i androgena sekrecija su pod kontrolom adrenokortikotropnog hormona hipofize (ACTH), dok je sekrecija aldosterona regulisana uglavnom preko sistema renin angiotenzin. ACTH stimuliše produkciju adrenalnog kortizola preko melanokortin 2 receptora (MC2R), takođe poznatog kao ACTH receptor (ACTHR), člana porodice G-protein sparenih receptora. Akutni odgovor nadbubrega na ACTH dešava se u toku sekunda do minuta, aktivacijom cikličnog adenozin monofosfata (cAMP) posredstvom StAR proteina, koji olakšava brzi priliv holesterola u mitohondrije. Hronična faza se odvija tokom nekoliko sati do dana i uključuje porast transkripcije adrenalnih enzima steroidogeneze.
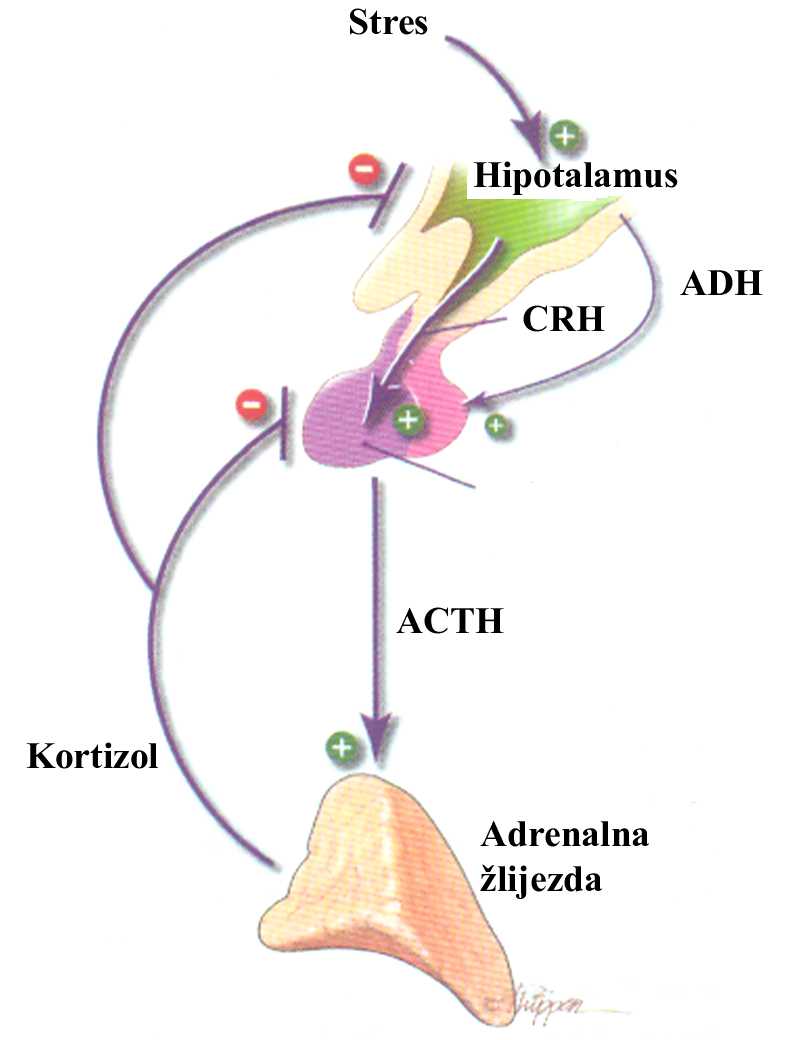
Sekrecija glikokortikoida je regulisana posredstvom tri mehanizma: kontrolom negativne sprege (koja je odgovorna za kontrolu izlučivanja kortikotropin-rilizing hormona-CRH), odgovorom na stres i danonoćnim (niktohemeralnim) ritmom. Lučenje kortizola je pod direktnom kontrolom adrenokortikotropnog hormona hipofize (ACTH), kojemu je nadređen kortikotropn-rilizing hormon hipot alamusa (CRH). CRH stimuliše izlučivanje ACTH iz prednjeg režnja hipofize u krv. ACTH stimuliše izlučivanje glikokortikoida, od kojih je kortizol kvantitativno najznačajniji. Povećane koncentracije kortizola u plazmi suprimiraju izlučivanje CRH, obratno, snižavanje kortizola u plazmi stimuliše sekreciju CRH. Smanjenjem sekrecije CRH smanjuje se i sekrecija ACTH, a preko ove glikokortikoida nadbubrežnih žlijezda (Slika).
alamusa (CRH). CRH stimuliše izlučivanje ACTH iz prednjeg režnja hipofize u krv. ACTH stimuliše izlučivanje glikokortikoida, od kojih je kortizol kvantitativno najznačajniji. Povećane koncentracije kortizola u plazmi suprimiraju izlučivanje CRH, obratno, snižavanje kortizola u plazmi stimuliše sekreciju CRH. Smanjenjem sekrecije CRH smanjuje se i sekrecija ACTH, a preko ove glikokortikoida nadbubrežnih žlijezda (Slika).
Od svih hormona nadbubrežnih žlijezda jedino kortizol ima sposobnost da putem negativne povratne sprege sprečava lučenje ACTH. ACTH djeluje na nadbubrežnu žlijezdu poslije vezivanja za receptor na ćelijskoj membrani. Mehanizmom negativne povratne sprege preko CRH kortizol inhibira sekreciju ACTH. Kada ACTH stimuliše sintezu polnih hormona u nadbubrežnoj žlijezdi, ovi ne inhibiraju njegovu sekreciju.
Odgovor na stres je takođe posredovan sa CRH i ACTH. Inicira se preko centara u CNS i kao posljedicu ima veliko povećanje izlučivanja hormona. Danonoćni (niktohemeralni) ritam koncentracije kortizola u plazmi odgovara individualnom dnevnom ritmu svake osobe.
Neposredni efekti stimulacije nadbubrega sa ACTH su povećano izlučivanje kortizola, androgena i estrogena. Do ovoga dolazi usled izlučivanja uskladištenih (presintetičkih) hormona, a efekti traju veoma kratko. Drugi neposredni efekti ACTH sastoje se u stimulaciji novih sinteza koje vode ka povećanom izlučivanju kortizola. Dugotrajni efekti ACTH stimulacije su povećanje osjetljivosti žlijezde na ACTH i hipertrofija kore nadbubrega.
Lučenje kortizola je cirkadijalno. Hipotalamusno-hipofizno-adrenalna osovina djeluje kao biološki sat. Sekrecija ACTH i kortizola i njihov nivo u plazmi se znatno povećava u ranim jutarnjim satima, a maksimum je izmedju 6 i 10 sati prije podne. Tokom poslijepodneva vrijednosti se smanjuju, a najniže su uveče i u toku noći. Cirkadijalni ritam lučenja kortizola se uspostavlja u uzrastu od 6 mjeseci. U cirkulaciji je 95% kortizola vezano za α2 globulin-transkortin ili corticosteroid binding globulin (CBG), a samo mali dio kortizola se veže za albumin. U uslovima normalne koncentracije kortizola u plazmi, samo mali njegov dio nalazi se u slobodnom stanju. Poluživot kortizola je 60-90 minuta. Eekskrecija kortizola se vrši preko urina u obliku 17-hidroksikortikosteroida. Izlučivanje čistog kortizola preko urina je malo, svega 1% od ukupne adrenalne produkcije.
Glavna uloga kortizola u normalnim fiziološkim koncentacijama je regulacija metabolizma ugljenih hidrata putem smanjivanja iskorišćavanja glikoze od strane ćelija, pod uticajem insulina, i stimulacijom glikoneogeneze u jetri. Medjutim, biološki učinci kortizola su daleko brojniji. Glikokortikoidi stimulišu diferencijaciju adipocita i podstiču kataboličke promjene u mišićima, koži i vezivnom tkivu. Kortizol smanjuje količinu bjelančevina, pospješuje mobilizaciju aminokiselina iz mišića i masnih kiselina iz masnog tkiva, ispoljava ketogeno djelovanje. Kortizol izaziva mobilizaciju masnih kiselina iz masti, ali se uprkos tome, u stanjima pretjerane sekrecije kortizola razvija jedan posebni oblik gojaznosti sa pretjeranim odlaganjem masti u predjelu trupa (trup kao u bizona) i glave (facies lunata). Taj tip gojaznsti nastaje usled pojačanog uzimanja hrane, tako da se u nekim tkivima mast čak brže stvara nego što se mobiliše i oksidiše. U stanjima akutnog stresa luči se povećana količina ACTH, a pod njegovim uticajem i kortizola. Nije sasvim razjašnjeno zašto se dešava to povećanje kortizola u stresu i koji su tu odbrambeni mehanizmi u pitanju. Takodje, ispoljava antiinflamatorno djelovanje, sprečava upalnu reakciju u alergijskim procesima, smanjuje broj eozinofila i limfocita u krvi. Kortizol povećava stvaranje eritrocita, mada mehanizam tog djelovanja nije sasvim jasan. U produženoj povećanoj sekreciji kortizola razvija se policitemija i obratno, kod smanjene sekrecije kortizola razvija se anemija.









Add comment