Antimikrobna rezistencija – podsjetnik o genezi problema
Prof. dr Gordana Mijović
Otpornost bakterija na antibiotike (antimirobna rezistencija, rezistencija) danas predstavlja ozbiljnu globalnu prijetnju zdravlju i opstanku ljudi, toliko veliku da se izjednačava sa prijetnjom koja dolazi od klimatskih promjena. Obje te opasnosti imaju neke zajedničke karakteristike – globalne su i potencirane su ljudskom aktivnošću.
Da bi moglo doći do pojave otpornosti bakterija na antibiotike najavio je još Aleksandar Fleming prilikom dodjele Nobelove nagrade (1945). On je tada rekao da nije teško podstaknuti rezistenciju kod bakterija ako se sa antibioticima ne rukuje pravilno. Paradoksalno, glavni podstrekač antimikrobne rezistencije jesu upravo antibiotici. Upravo jedini ljekovi koji mogu da spriječe rast i razmnožavanje bakterija, pa čak i da ih ubijaju, omogućavaju bakterijama da u njihovom prisustvu preživljavaju.
Otpornost na neke antibiotike je prirodno svojstvo nekih bakterija. Tako npr. mikoplazme su rezistentne na beta-laktamske antibiotike, jer nemaju ćelijski zid. Beta-laktamski antibiotici uništavaju bakterije tako što onemogućavaju sintezu bakterijskog ćelijskog zida, kojeg mikoplazme prirodno nemaju. Kad se govori o problemu rezistencije na antibiotike misli se na problem stečene rezistencije. To je rezistencija bakterija koje su prirodno osjetljive na neke antibiotike, ali su sticajem okolnosti postale rezistentne.
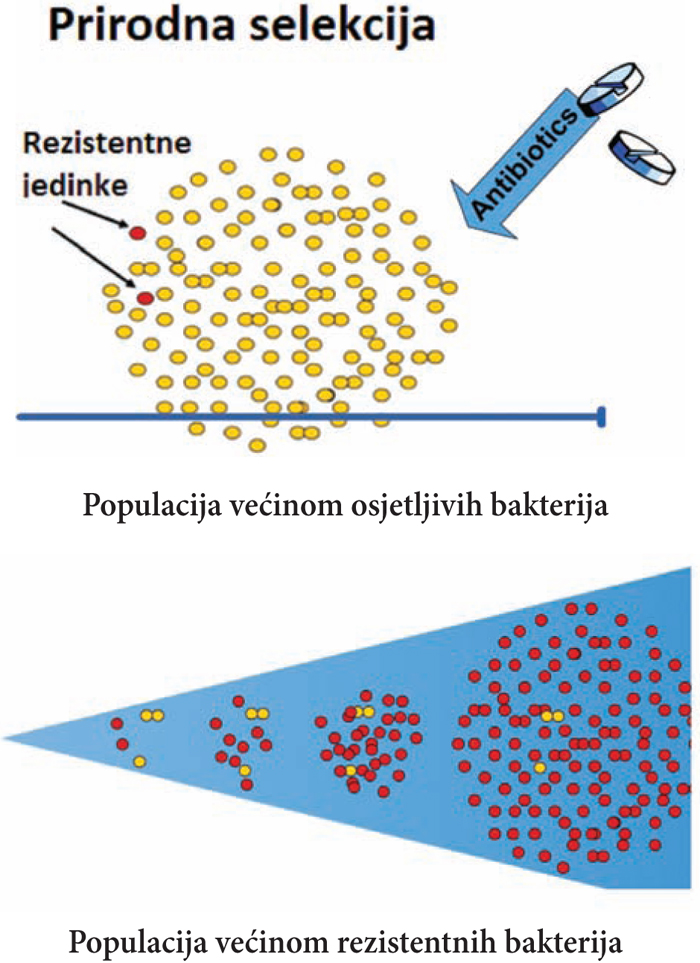
Sl.1 Selektivni pritisak antibiotika
Na ilustraciji je prikazana populacija divljeg (izvornog) soja bakterija koje su u svom prirodnom stanju osjetljive na određeni antibiotik. Kao u svakoj drugoj populaciji, i ovdje se javljaju pojedinačne, „drugačije“ jedinke, koje su mutacijama ili drugim putem postale rezistentne na taj antibiotik, ali se nalaze okružene brojnim jedinkama prirodnog, neizmjenjenog stanja (slika 1). Te bakterije koje su u neizmjenjenom, prirodnom stanju su, samim tim, mnogo životno potentnije od bakterija oštećenih mutacijama ili opterećenih plazmidima. Ne samo da postoji razlika u životnom potencijalu nego i u brojnosti. Ove prirodne, osjetljive jednike drže pod kontrolom mnogo manje brojne izmjenjene jedinke, pošto kao brojnije lakše dolaze do hrane, vlage i faktora rasta. Međutim, ako se djeluje antibiotikom i uništi populacija osjetljivih bakterija (ili značajno smanji njihov broj), onda one rezistentne više nemaju konkurenciju, pa iako manje vrijedne, rezistentne jedinke počinju nesmetano da se razmnožavaju. Ovo rezultira time da iz populacije većinom na antibiotik osjetljivih, dobijemo populaciju većinom rezistentnih bakterija.
Istraživanja su potvrdila da kod bakterija postoje geni rezistencije na antibiotike i prije prve kliničke upotrebe antibiotika. Ispitivano je prisustvo gena rezistencije u sojevima koji su u prošlosti pohranjeni u banku sojeva. U sojevima pseudomonasa iz 2005. nađeni su geni rezistencije na imipenem/relebaktam, koji je tek 2019. počeo da se koristi u kliničkoj praksi. Prvi slučajevi infekcije izazvane takvim pseudomonasom prijavljeni su već 2020. To opominje da se mora računati na prisutnost u prirodi bakterija sa genima rezistencije za neke buduće antibiotike i strategiju kontrole širenja otpornosti bakterija na antibiotike prilagodiri tome.
Bakterijski internet
Postavlja se pitanje kako tako naglo dođe do širenja antimikrobne rezistencije u bakterijskoj populaciji? Koliko treba čekati da se nakon početka primjene nekog antibiotika i pojave rezistentnih sojeva, rezistencija raširi među bakterijama? Nažalost, ne mnogo, bar za neke oblike rezistencije. Bakterije su vrlo dobro opremljene svojim internetom – plazmidi su njihov internet.
Plazmidi su samostalni mali genetski elementi koji se nalaze u bakterijama i koji imaju sposobnost da se umnožavaju nezavisno od toga da li se bakterija dijeli ili ne.
Bakterije imaju sposobnost da kopije plazmida koji mogu da nose, između ostalog, i gene za rezistenciju, podijele svojim “komšinicama”. One ih isporučuju susjednim bakterijama koje čak ne moraju biti ni istog roda, a mogu biti i vrlo genetski udaljene bakterije. Na ovaj način se informacija o rezistenciji širi horizontalno (Slika 2). Međutim, istovremeno, kada se bakterije dijele, one kopiju plazmida predaju i ćelijama kćerkama, pa na taj način informacija o rezistenciji se širi vertikalno. Zato se može reći da su plazmidi bakterijski internet.
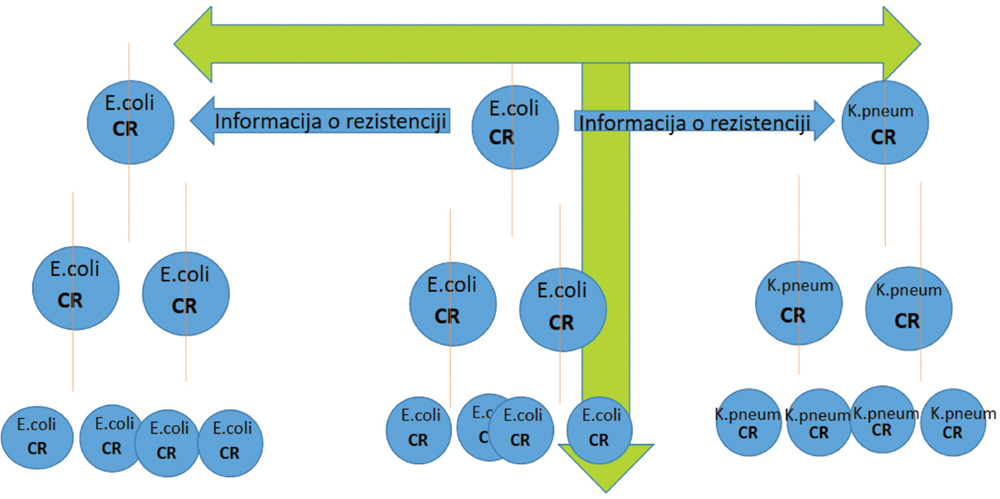
Sl. 2 Plazmidi: bakterijski internet
Plazmidi su, inače, specijalnost gram-negativnih bakterija i danas u svijetu najveća je zabrinutost stručne javnosti zbog rezistencije gram-negativnih bakterija. S gram-pozitivnim bakterijama je nešto drugačija situacija i one mogu da posjeduju plazmide, ali su oni manje prisutni kod njih. Recimo, rezistencija na meticilin u Staphylococcus aureus-u je vezana za hromozom. Ako se geni rezistencije nalaze na hromozomu, njihovo prenošenje je dominantno vezano za dijeljenje bakterija. Rezistencija Staphylococcus aureus-a na penicilin i meticilin je slikovit primjer razlike u brzini propagiranja neke rezistencije, zavisno od toga da li se geni za rezistenciju nalaze na plazmidu ili se nalaze na hromozomu.
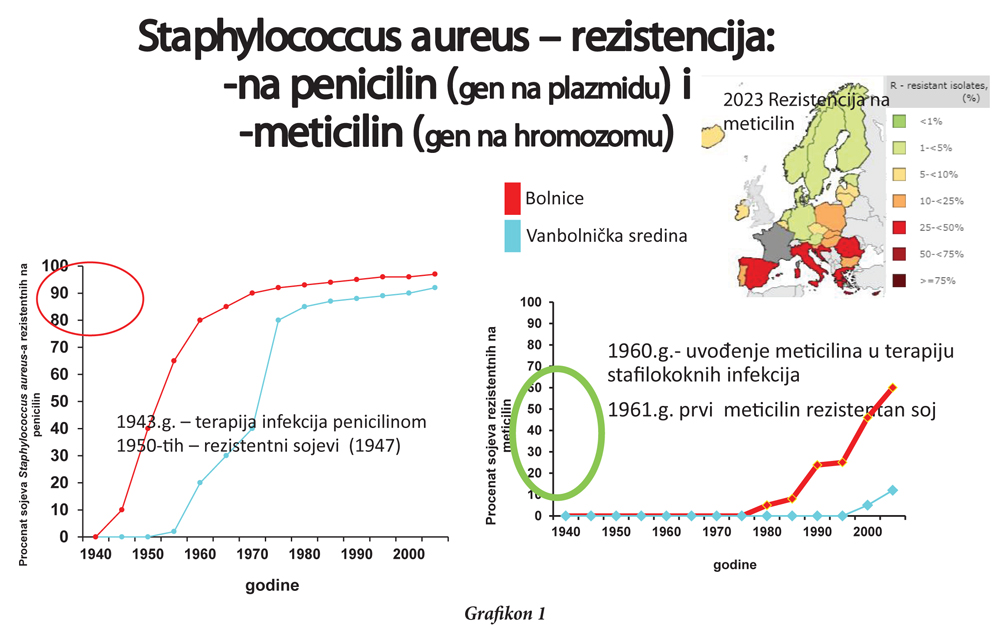
Penicilin je uveden u terapiju 1943, a u 50-im godinama je zabilježena pojava rezistentnih sojeva, pri čemu je stopa rezistencije rasla geometrijskom progresijom.
Logično da su se prvi sojevi Staphylococcus aureus-a rezistentnih na penicilin pojavili u bolnicama, zato što su bolnice mjesta gdje su u kontinuitetu prisutni antibiotici, koji se daju bilo terapijski, bilo profilaktički. Nakon 10-tak godina rezistencija na penicilin počela je da se javlja i u vanbolničkoj sredini. Grafikon pokazuje kako je geometrijskom progresijom stopa rezistencije na penicilin porasla za kratak period vremena i već 60-tih penicilin je postao neupotrebljiv za liječenje stafilokoknih infekcija (grafikon 1). Danas je stopa rezistencije stafilokoka na penicilin između 80 i 100%, globalno.
Meticilin je uveden u terapiju 60-ih godina prošlog vijeka. Što se tiče otpornosti na meticilin, koja se, takođe, pojavila relativno brzo nakon njegovog uvođenja u terapiju, može se reći da se ta rezistencija ipak sporije širila. Ona se prenosi genima koji se nalaze na hromozomu.
Postoje zemlje koje drže na vrlo niskom nivou stopu rezistencije na meticilin, čak ispod 5%. To su skandinavske zemlje i zemlje Sjeverozapadne Evrope, gdje se, inače, već decenijama vodi ozbiljan program nadzora upotrebe antibiotika i antibiotici se vrlo restriktivno koriste (slika 3).
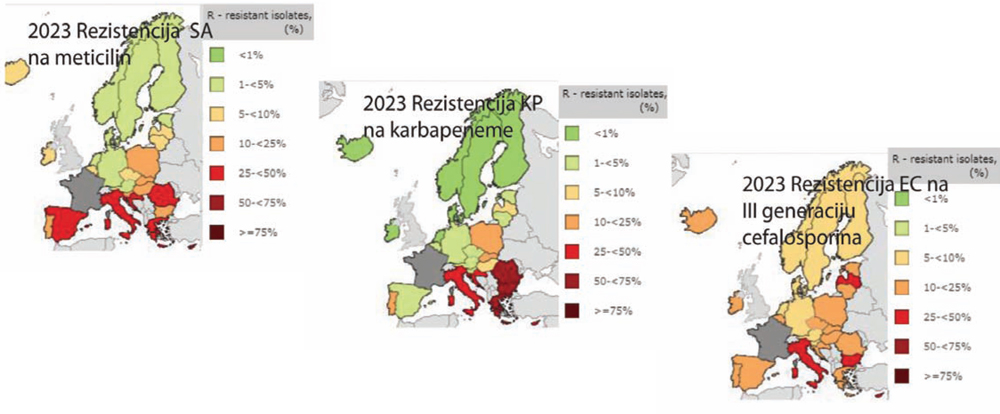
Sl. 3 EARS-net prikaz rasprostranjenosti antimikrobne rezistencije u Evropi (2009/2023)
Skini grafikon donji sa državama i stranim tekstom ispod grafikona
Svjetska zdravstvena organizacija je napravila listu prioritetnih patogena koji se po pitanju rezistencije smatraju potencijalnim problemom za javno zdravstvo. Gram-negativne bakterije su svrstane u kritičnu grupu po tom pitanju, upravo zbog načina i brzine propagiranja rezistencije kroz bakterijsku populaciju, dok Gram-pozitivne bakterije uglavnom spadaju u srednje rizičnu grupu.
Kako je došlo do ovakvog razvoja događaja? Pogled unazad govori da je prošlo zlatno doba antibiotika koje je trajalo između 50. i 70. godina 21. vijeka. U tom periodu su praktično osmišljeni svi antibiotici koji se danas koriste. Poslednji su bili karbapenemi (1985), a kasnije dolaze uglavnom modifikacije postojećih grupa i već poznatih mehanizama djelovanja antibiotika.
Zašto nema intenzivnije produkciju novih antibiotika sa novim mehanizmima djelovanja? Jedan razlog je taj što farmaceutske kuće nisu zainteresovane za antibiotike. Dugotrajan je proces njihovog istraživanja, potrebna su dugoročna ulaganja, koja se sporo vraćaju, jer su to su ljekovi za jednokratnu upotrebu (najčešće samo dok traje infekcija). Srećom, Evropska komisija svojim subvencijama podstiče farmaceutske kuće u istraživanjima novih antibiotika. Drugi razlog je što su bakterije vrlo jednostavni mikroorganizmi. Jako je malo mjesta u njima koja mogu biti cilj antibiotika. Praktično su sva iskorištena: ćelijski zid, citoplazmatska membrana, ribozomi i hromozom. Na to, naravno, ne možemo uticati, ali se nastavljaju intenzivna ispitivanja u pravcu pronalaženja nove mete za antibiotike i novog mahanizma djelovanja.
Ipak, šta je svijetlo na kraju tunela? Svijetlo na kraju tunela je to što je dokazano da postoji reverzibilnost procesa. Ako neki antibiotik nije u upotrebi određeno vrijeme, osjetljivost na njega može da se vrati. Zapravo, kada uklonite antibiotik, dajete šansu onim pojedinačnim preostalim osjetljivim jedinkama sa većim životnim potencijalom da se nametnu, da potisnu rezistentne jedinke i da se kroz neko vrijeme (u pitanju su godine) ponovo uspostavi većinska populacija osjetljivih bakterija (slika 4).
Zemlje Skandinavije i Sjeverozapadne Evrope, gdje se antibiotici vrlo restriktivno koriste, dokazuju da je moguće pažljivim rukovanjem antibioticima držati rezistenciju na niskom nivou.
Šta god činili, valja imati na umu da svijet ne završava sa nama, već slijede nove generacije kojima ne smijemo da ukinemo antibiotike. Moramo da razmišljamo o tome da će i njima biti potrebni ovi dragocjeni ljekovi, a na nama danas je odgovornost da im to omogućimo. Uspješnost borbe za očuvanje i vraćanje efikasnosti antibiotika zavisi od svih nas. Svako može dati svoj doprinos toj borbi odgovornim odnosom prema antibioticima.
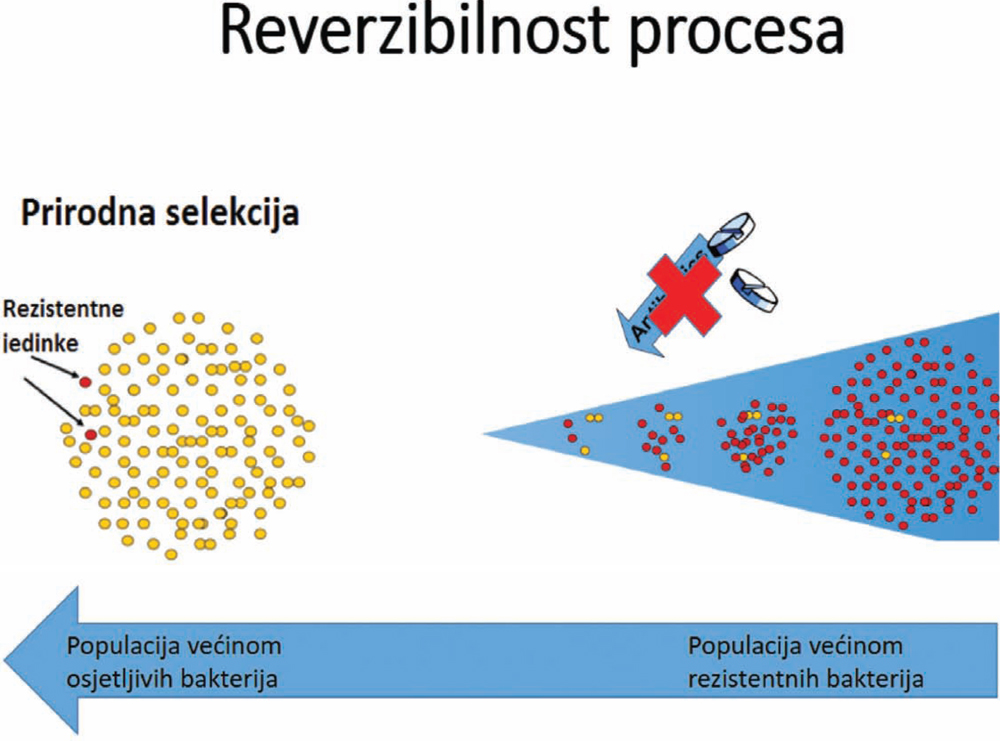
Sl 4. reverzibilni proces: vraćanje osjetljivosti na neki antibiotik