Relapsi bolesti pri haploidentičkoj transplantaciji u klasičnoj potpunoj HLA alogenskoj transplantaciji i haploidentičkoj transplantaciji sa selektivnim smanjenjem αβ + T-ćelija su slični. Ako potpuno depletiramo sve T-ćelije, imamo veći stepen relapsa, tako da moramo biti selektivni u tome. Zadržavanje γδ + T ćelija štiti GVL efekat. Slijedi efekat zadržavanja γδ + T ćelija. Ako ih ostavite na niskom nivou — imaju veliki uticaj na preživljavanje, ali ako ih depletirate — pacijent može biti izgubljen. Količina kumulativnog relapsa HLA veoma je slična u različitim vidovima transplantacija i iznosi 20-22%. Procenat oporavka u navedenom istraživanju je 52%, ali moramo biti iskreni i priznati da je ovo veoma selektivna studija. Ovaj procenat može biti manji, oko 45%, ali veliki broj nesrodnih donatora i HLA T-ćelija ima simbolične nedostatke i njihov broj se kreće oko 45%.
Koji su budući pravci za ponovno pojavljivanje bolesti nakon transplantacije? Možemo da koristimo infuzije αβ i T-ćelija depletiranih donorskih limfocita, T-reg i manipulaciju suicidnim genom u slučaju kada postoji GVHD koji ugrožava život poslije T-ćelijske terapije ili DLI-a, himernog receptora antigena (CAR), T-ćelijske terapije i Bi-specifičnih T-ćelijskih angažmana. Ako uništite T-ćelije na taj vrlo inteligentan visokotehnološki način, možete uništiti tumor, na primjer. Ovo je budućnost terapije tumora.
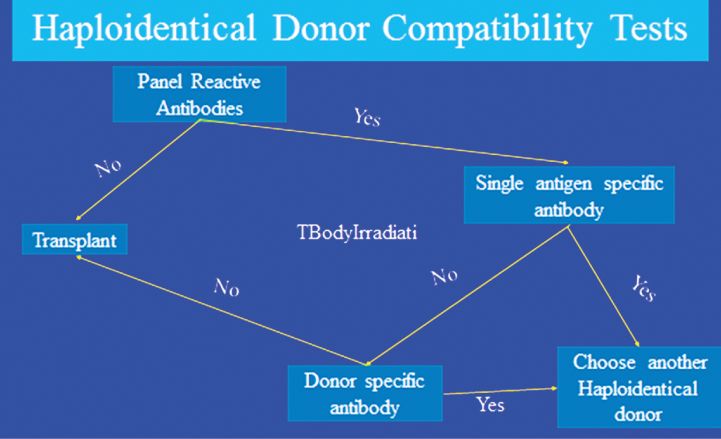
Samo zato što neko ima majku ili oca ili haploidentičnu sestru, brata ili dijete koji može biti donator, ne znači da on automatski može ići na transplantaciju. Sprečavanje odbacivanja grafta u haploidentičkoj transplantaciji trebalo bi, za početak, da bude obrađeno testovima kompatibilnosti, nakon čega je moguće uzeti megadozne matične ćelije od donatora mezenhimalnih matičnih ćelija. Haploidentični testovi kompatibilnosti donatora koriste se za snimanje reakcije antitijela. Ukoliko pacijent ima antitijela, potrebno je sprovesti testiranje u vezi sa tim da li ona predstavljaju prijetnju antigenima donatora. Ako predstavljaju, onda ćemo promijeniti donatora.
 Slika 1: Haploidentička donatorska kompatibilnost
Slika 1: Haploidentička donatorska kompatibilnost
Druga bitna stvar je smrtnost uzrokovana infekcijama u haploidentičkoj transplantaciji. To je najveći izazov, jer posebno u novije vrijeme većina smrtnih slučajeva u vezi je sa infekcijama, najčešćim uzrokom smrtnosti bez relapsa. Pojavljuje se kao rezultat spore imunološke rekonstitucije koja može trajati godinu dana ili više. Imunska disfunkcija u haploidentičkoj transplantaciji kod odraslih uzrokovana je propadanjem timusne funkcije. Imunološki oporavak nakon transplantacije zavisi, naročito u roku od mjesec dana, od ekspanzije zrelih T-ćelija unešenih u graft. Pacijent se kod nemanipulisane haplo-HSCT periferne ekspanzije T-ćelija priprema antagonizovanom imunološkom supresivnom terapijom. U Haplo-HSCT depleciji T-ćelija repertoar T ćelija je veoma mali, pa zbog malog broja T-ćelija u graftu i ATG u uslovima kondicioniranja dovodi do dodatne in vivo T-ćelijske deplecije. U oba slučaja imamo imunsku disfunkciju.
U roku od nekoliko mjeseci nakon haploidentičke transplantacije moguć je spori oporavak antimikrobnih i antivirusnih odgovora i osjetljivost na opasne oportunističke infekcije. Infekcije u haploidentičkoj transplantaciji obično su bakterijske: infekcije krvotoka (Pseudomonas, E. Coli, Klebsiella — paziti na višestruku antibiotski rezistentnu formu), pneumonija, gastrointestinalni tifilitis zbog Enterococci i Clostridium difficle. Od invazivnih gljivičnih infekcija uočene su: Aspergillosis (81%), Candidiasis (11%), Zygomycosis (4%), Fusariosis (2%). Aspergillus je uobičajen kod pacijenata sa haploidentičkim transplantatom (do 27%). Preporuka je da se vodi računa o tome da je gljivična infekcija rezistentna na vorikonazol — obično osjetljiva na lipozomalni amfotericin B. To izaziva visoku učestalost pojave GVHD-a.
Virusne infekcije su uzrokovane: CMV-om, EBV-om, adenovirusom (lokalno npr. hemoragični cistitis, kolitis, pneumonija ili diseminovano), polioma BK virusom (hemoragični cistitis), HHV-6. Od parazitima izazvanih bolesti možemo da apstrahujemo: groznicu, limfadenopatiju, meningitis, moždani apsces, pneumonitis, miokarditis, hepatitis, pancitopeniju itd. Ovdje su posebno rizične transplantacije deplecijom T-ćelija.
Reaktivacija Epštajn-Barovog virusa uzrok je značajnog morbiditeta i smrtnosti kod haploidentičkih transplantata. EBV indukovani limfomi obično potiču iz donorskih B ćelija, ali mogu poticati i od primaoca. Deplecija CD 19+ ćelija donora značajno smanjuje reaktivaciju EBV-a i time smanjuje učestalost pojave limfoma koji proizilaze iz ove komplikacije, koji su često pogubni.
T-ćelije specifične za virus u HLA veoma su fascinantna pojava. Adoptivni prenos donorskih patogen specifičnih citotoksičnih T-limfocita protiv CMV-a, EBV-a, adenovirusa, Aspergillusa može efikasno obnavljati imunitet protiv specifične infekcije kod 70-90% pacijenata. Niska stopa GVHD-a daje trajne odgovore. Oni traju dugo. Ako nedostatak imuniteta kod donatora blisko odgovara trećoj strani, VST-ovi se mogu infuzirati sa stopom odgovora od 60-70%.
Naša iskustva
CD45 Ra T-ćelija je veoma zanimljiva stvar u transplantaciji. Studije pokazuju da su CD45 Ra T-ćelije odgovorne za GVHD. Stoga bi deplecija ovih ćelija, teoretski, trebalo da prevaziđe problem T-ćelija koje su odgovorne za antivirusnu aktivnost. Ove antivirusne T-ćelije mogu se koristiti za liječenje reaktivacije nakon transplantacije CMV-a i EBV infekcija. Osim toga, profilaktička primjena transplantata donatorskih antivirusnih T-ćelija pacijentu treba da obezbijedi protivvirusni imunitet pacijentu.
Iskustvo deplecije CD45 Ra T-ćelija u Altunizade Acıbadem bolnici stečeno je u vezi sa 11 pacijenata kod kojih je reaktiviran CMV u post haplo transplantaciji. Postojao je progresivan porast titara CMV-a uprkos tome što je sprovođeno liječenje ovih pacijenata. CD45 Ra T-ćelijska deplecija mononuklearnih ćelija vršena je kod donatora svakog pacijenta. Svih 11 pacijenata postali su CMV negativni u roku od 10 dana od primjene antivirusnih T-ćelija. Isti ishod se očekuje u liječenju EBV-a i adenovirusnih infekcija sve dok je antivirusni imunitet donatora protiv ovih virusa prisutan. Ako vaš donator nije EBV ili na drugi način pozitivan, ne možete da koristite ovaj tretman.
Pogledajmo rezultate αβ + T ćelija, antigen prezentujućih ćelija i depleciranih CD19 + ćelija i profilaktičke mezenhimalne matične ćelije koje pokazuje haploidentička transplantacija. Imali smo 25 pacijenata. Prosječni monitoring trajao je godinu dana. Nakon transplantacije nije bilo imunosupresije ljekovima. Podaci o haploidentičkom transplantatu pokazuju da su neutrofili veći od 500 / mL, trombociti većih od 20000 / mL, a signifikantno je i trajanje neutropeničke groznice. Reaktivacija CMV-a bila je vrlo česta virusna infekcija 10/25 (40%). Relaps bolesti imao je ukupno preživljavanje od 100 dana, i ovo je istorijski detalj. Vid. tabelu sa pojedinostima.
 Tabela 1: Podaci o haplontoidentičkoj transplantaciji Tabela 1: Podaci o haplontoidentičkoj transplantaciji |
|
Zaključak u vezi sa haploidentičkim transplantacijama izvedenim posredstvom αβ + T ćelija, CD 19+ ćelije, antigen prezentujućih ćelija i mezenhimalnih matičnih ćelija jeste da imamo efektivne rezultate. Evidentno je značajno smanjenje GVHD-a. Stopa relapsa nije povećana u poređenju sa ranijim kontrolama. Kratkoročan je engraftment neutrofila i trombocita, smanjeno trajanje boravka u bolnici, poboljšan status bolesnika u odnosu na hemioterapiju / TBI za haploidentičku transplantaciju i infuziju T-ćelija donatora. Nakon deplecije CD45R-a imamo visoko obećavajući tretman za reaktivaciju CMV-a i imunorekonstituciju i terapiju protiv drugih virusnih infekcija.
Prevod, Anita Đurović
[1] (BMT CTN Protocol 303, Devine S et al, BBMT 2011)
Prof. dr Siret Ratip,
Odjeljenje za hematologiju,
Bolnica Altunizade Acibadem, Istanbul









Add comment