Dr Maja Kavarić, pedijatar hematolog
Institut za bolesti djece, Klinički centar Crne Gore
Savremena medicina svakim danom nastoji bolesnicima pružiti najbolju njegu razvojem novih terapija i ljekova. Posljednjih decenija postignut je izvanredan napredak u liječenju malignih bolesti, kako odraslih, tako i djece.
Imunoterapija karcinoma predstavlja novi oblik liječenja i novu nadu za oboljele pacijente. U proteklih nekoliko godina imunoterapija se pojavila kao „peti stub“ terapije kancera. Ovaj vid liječenja stimuliše naš imuni sistem da uništava ćelije raka. Imuni sistem ljudskog organizma je podešen tako da prepoznaje strane ćelije. To mogu biti bakterije, virusi, ali i maligne ćelije. Usljed kompleksne regulacije imunog sistema ove ćelije nekad mogu da prođu neopaženo našim imunim ćelijama i nakon toga se razmnožavaju i formiraju maligni tumor i metastaze.
2017. godine je odobren prvi „živi lijek“ za terapiju raka. Američka agencija za hranu i ljekove (FDA – Food and Drug Administration) je odobrila prvi lijek koji redizajnira imunološki sistem samog pacijenta, tako da može da napada ćelije raka. “Živi lijek“ se priprema tako da je specifičan za svakog pacijenta ponaosob, za razliku od konvencionalnih terapija, odnosno operativnog liječenja, hemio ili radioterapije.
Prvi „živi lijek“ se zove CAR-T ili Himera Antigen receptor T-ćelija (Chimeric Antigen receptor T-cell). To je nova vrsta imunoterapije, koja najviše obećava kod različitih vrsta raka krvi, odnosno, trenutno se koristi u svijetu za određene tipove leukemija i limfoma. Istraživanja su pokazala da je efikasna i kod multiplog mijeloma, kao i kod karcinoma pluća i malignog melanoma.
Do sada su agencije za ljekove poput američke FDA i evropske EMA (European Medicines Agency) 2017. i 2018. godine obobrile dva lijeka na principu ove terapije: tisagenlecleucel je terapija autolognim (sopstvenim) T ćelijama, koje su dobijene lentivirusnim vektorom i kodiraju anti CD-19 CAR koji specifično prepoznaje CD-19 antigen na B ćelijama. Koristi se za liječenje osoba sa akutnim B ćelijskim leukemijama i B ćelijskim limfomima. Drugi lijek axicabtagene ciloleucel je slična terapija, ali su anti CD-19 CAR-T ćelije dobijene retrovirusnim vektorom. Ova terapija je namijenjena odraslim bolesnicima sa B ćelijskim limfomima.
Širom svijeta su već prihvaćeni brojni ljekovi koji „kidaju kočnice“ sa imunog sistema kako bi mu omogućili da lakše napadne ćelije raka. CAR –T tehnologija ide korak dalje, redizajnirajući imuni sistem na mnogo specifičnijem nivou. Važno je naglasiti da svaka individualna terapija CAR-T ćelijama ima jedinstven dizajn i proces proizvodnje, bez obzira što su svi zasnovani na istom principu. Zato se ove trapije mogu davati jedino u specijalizovanim centrima od strane dobro obučenog medicinskog tima. Terapija CAR-T ćelijama je novi lijek, dokazano efikasan, ali za sada dosta skup. Zato je terapija odobrena u malom broju zemalja, a u mnogim zemljama je pacijenti dobijaju kroz kliničke studije.
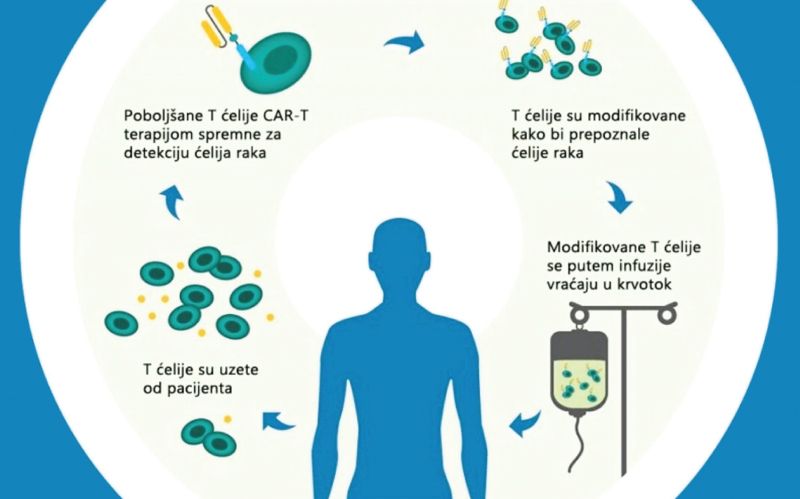
Protokol terapije CAR-T ćelijama
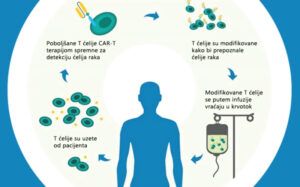 Proces proizvodnje CAR-T ćeija sadrži više kompleksnih koraka. Pacijenti koji zadovoljavaju kriterijume za primanje CAR-T ćelija imaće inicijalni razgovor sa svojim hematologom, gdje će im biti predočeno šta mogu da očekuju prije, u toku i nakon procesa primanja pomenute terapije. Postupak se obavlja uz pristanak pacijenta. Ukoliko je pacijent pravi kandidat, tim za liječenje određuje termin za leukoferezu. Leukofereza je postupak gdje se pomoću aparata iz krvi davaoca izdvajaju leukociti, odnosno T limfociti, a ostatak krvi vraća pacijentu. Ovaj proces zahtijeva da pacijent ostane miran u periodu od 3-6 sati.
Proces proizvodnje CAR-T ćeija sadrži više kompleksnih koraka. Pacijenti koji zadovoljavaju kriterijume za primanje CAR-T ćelija imaće inicijalni razgovor sa svojim hematologom, gdje će im biti predočeno šta mogu da očekuju prije, u toku i nakon procesa primanja pomenute terapije. Postupak se obavlja uz pristanak pacijenta. Ukoliko je pacijent pravi kandidat, tim za liječenje određuje termin za leukoferezu. Leukofereza je postupak gdje se pomoću aparata iz krvi davaoca izdvajaju leukociti, odnosno T limfociti, a ostatak krvi vraća pacijentu. Ovaj proces zahtijeva da pacijent ostane miran u periodu od 3-6 sati.
Produkt leukofereze se šalje u pogon za proizvodnju CAR-T ćelija. To su specijalno dizajnirane laboratorije, gdje se in vitro genetski modifikuju CAR-T ćelije. U laboratorijama, uz pomoć neaktvnog virusa (lenti li retrovirusa), himera antigen receptor je ubačen u T ćelije pacijenta. Tako nastala ćelija bolje i efikasnije prepoznaje i ubija ćeliju kancera. Ovo je, kao što smo predhodno rekli, „živi lijek“, što znači da kada CAR-T ćelija pronađe ćeliju raka i uništi je ona ne umire, već nastavlja da ubija nove maligne ćelije.
Broj CAR-T ćelija koje se vraćaju u organizam pacijenta je veliki, tako da vrijeme potrebno za proizvodnju CAR-T ćelija može trajati nekoliko nedjelja i varira između tri do sedam nedjelja. Kada se proizvede dovoljan broj ćelija one se zamrzavaju i transportuju nazad u bolnicu, odnosno centar gdje će se procedura obaviti. Zamrznute ćelije, ukoliko se adekvatno čuvaju, mogu stajati više od godinu dana i ne moraju se odmah koristiti.
Pacijenti prije vraćanja genetski modifikovanih CAR-T ćelija primaju niske doze hemioterapije, u cilju smanjena broja drugih imunih ćelija. Ova terapija obično se daje od 2-14 dana prije infuzije CAR-T ćelija. Tip hemioterapije i doza se razlikuju od pacijenta do pacijenta.
Pacijent se nakon toga poziva u specijalizovani klinički centar, gdje se obavlja procedura. CAR-T ćelije se putem intravenske infuzije vraćaju pacijentu. Ovaj proces traje od 30-60 minuta. Sve vrijeme je pacijent pod strogim nadzorom čitavog tima ljekara. Nakon infuzije CAR-T ćelija pacijenti ostaju u bolnici najmanje dvije sedmice ili duže, zato što se neželjeni efekti javljaju obično između drugog i sedmog dana.
Po napuštanju bolnice, pacijentima se savjetuje da sljedeća najmanje dva mjeseca od infuzije ostanu u blizini centra gdje je procedura rađena, kako bi u slučaju komplikacija mogli da se jave u Hitnu službu za manje od dva sata. Pacijenti dolaze u narednih godinu dana na redovne kontrole u tačno određeno vrijeme, a prate se narednih deset godina.
Nedostaci CAR-T ćelijske terapije:
– citokinska oluja i
– encefalopatija.
CAR-T ćelijska terapija svojim djelovanjem u tijelu bolesnika dovodi do nuspojava. Najčešće nuspojave uključuju infekcije, oštećenje pluća, kardiovaskularnog i nervnog sistema. Jedna od njih je sindrom oslobađanja citokina-CRS (cytokine release syndroma) ili citokinska oluja. Znakovi citokinske oluje se javljaju u prvih 14 dana nakon infuzije. Kao prvi simptom CRS se javlja povišena temperatura, groznica, takikardija, hipotenzija, može doći i do zatajenja disanja i respiratorne insuficijencije.
Takođe, CAR-T ćelije mogu štetno uticati i na više drugih organa, jetru, bubrege -bubrežna insuficijencija, mogu dovesti do citopenije i DIK-a (diseminovana intravaskularna koagulacija).
Neurološke komplikacije se jednim imenom nazivaju sindrom encefalopatije povezan sa CAR-T ćelijama (CRES, tj CAR-T cell related encephalopathy syndrome) i on se može pojaviti zajedno ili odvojeno od citokinske oluje, nekad i nakon više sedmica od davanja infuzije.
Liječenje nuspojava
Za smanjenjenje nuspojava koriste se imunosupresivni ljekovi. Srednji do teški oblik citokinske oluje liječi se tocilizumabom, anti –IL-6 antitijelom, antagonistom receptora za IL-6. Tocilizumab je u mnogim slučajevima pokazao brzo i potpuno smanjenje nuspojava. Pojedini teški slučajevi zahtijevaju uz tocilizumab i primjenu kortikosteroida. Osim toga, liječenje uključuje terapiju antibioticima širokog spektra, faktore rasta, transfuzije i drugu potpornu terapiju.
Budućnost CAR-T ćelijske terapije
Budućnost CAR-T ćelijske terapije bile bi unverzalne CAR-T ćelije. Novi oblici CAR-T ćelija izrađuju se sa namjerom povećanja fleksibilnosti i širenja mogućnosti prepoznavanja antigena. Stvaranje univerzalnih CAR sa gotovo beskonačnom sposobnošću prepoznavanja antigena uključuje neki oblik posredničkog sistema koji će povezivati ciljni antigen kancera i antigen specifičnu jedinicu CAR-a.
Potrebno je još jednom naglasiti, da je na sadašnjem nivou, liječenje CAR-T ćelijama rezervisano samo za određenu grupu hematoloških pacijenata:
– osobe sa B ćelijskom akutnom limfoblastnom leukemijom koja je refrakterna na terapiju, u recidivu nakon transplantacije ili u drugom ili kasnijem recidivu,
– odrasle osobe sa recidivirajućim ili refrakternim difuznim, krupnoćelijskim B ćelijskim limfomom (DLBCL), nakon dvije ili više linija sistemske terapije.
Primjena CAR-T terapije u državama regiona je započeta u Hrvatskoj i Sloveniji. Kliničko-bolnički centar Zagreb je prva bolnica u ovom djelu Evrope koja je 2019. godine počela liječenje personalizovanom CAR-T-terapijom, a 2020. godine im se pridružio i Univerzitetski centar Ljubljana. Do sada su ukupno imali 15 pacijenata, od kojih dvoje djece sa akutnom limfoblastom leukemijom, a ostalo su bili odrasli pacijenti sa difuznim, krupnoćelijskim B limfomom.
Imunoterapija karcinoma, zbog svoje efikasnosti, dugotrajne kontrole raka i dužeg preživljavanja bolesnika, postaje najvažnija terapija u liječenju malignih bolesti. Jednom riječju, u liječenju raka počela je nova era – era imunoterapije.








Add comment