Mr sci Danijela Đurović Raonić, spec. oftalmologije
Klinički centar Crne Gore
Senilna makularna degeneracija (AMD/ARMD) jedan je od vodećih uzroka sljepila u razvijenom svijetu kod ljudi starosti preko 50 godina. Prevalencija bolesti je u porastu, te se procjenjuje da će broj bolesnika u svijetu od trenutnih 196 milona porasti na gotovo 300 miliona u 2040. godini.
AMD je multifaktorijalna bolest s prisutnom genetskom komponentom. Prema istraživanjima do sada su identifikovane 52 varijante na 34 genska fokusa kao nezavisni prediktori AMD. Pri tom je starost identifikovana kao najsnažniji faktor rizika i gotovo svi slučajevi kasne AMD zabilježeni su kod osoba starijih od 60 godina, češće kod bijele rase. Ostali faktori rizika su konzumiranje cigareta koje udvostručuje rizik, nutritivni faktori i kardiovaskularne bolesti.
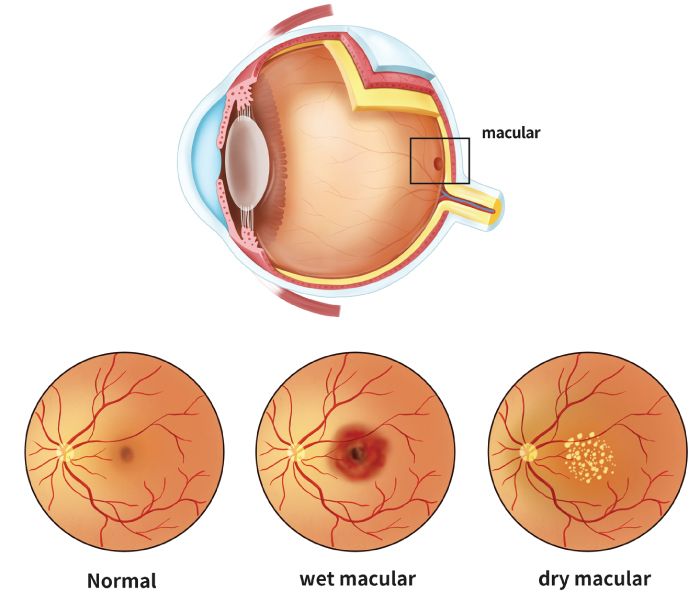
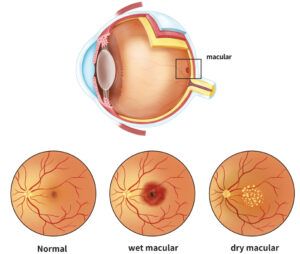 Postoje dva oblika AMD, suvi (dry) i vlažni (wet). Suvi oblik (rani stadijum) obilježen je poremećajem retinalnog pigmentnog epitela i fokalnim nakupinama metaboličkih nusproizvoda koje nazivamo druze.
Postoje dva oblika AMD, suvi (dry) i vlažni (wet). Suvi oblik (rani stadijum) obilježen je poremećajem retinalnog pigmentnog epitela i fokalnim nakupinama metaboličkih nusproizvoda koje nazivamo druze.
Približno 90% bolesnika s AMD ima ovaj oblik. Suvi oblik često je asimptomatski, a pogoršanje centralnog vida kod takvih bolesnika obično se razvija sporo. Neki bolesnici primijete centralnu distorziju, posebno pri čitanju, te otežano čitanje pri slabijoj osvijetljenosti. Za suvi oblik ne postoji utvrđena terapija, no poznato je da primjena antioksidansa kod osoba s AMD može smanjiti progresiju prema uznapredovalim stadijumima (AREDS 2001, AREDS 2014). Preopručuje se i samokontrola Amslerovom rešetkom, te prekid pušenja i metabolička regulacija (smanjenje gojaznosti, kontrola krvnog pritiska). Preporučena suplementacija po AREDS 2 studiji je u sljedećim dozama: vitamin E (400 IU), vitamin C (500 mg), lutein (10 mg), zeaxantin (2 mg), cink (25–80 mg); manja doza može imati isti efekat), bakar (2 mg).
Kasni stadijum AMD može biti atrofični (suvi, ne-eksudativni; geografska atrofija) ili vlažni (takođe poznat kao neovaskularni ili eksudativni oblik). Vlažni oblik (prisutan u približno 10% bolesnika) obilježen je ubrzanim propadanjem centralne vidne oštrine usljed abnormalnog rasta krvnih sudova iz horoidalnog sloja (horoidalna neovaskularizacija – CNV) u subretinalni prostor. Mogu se razlikovati različiti tipovi CNV-a u vlažnoj AMD: tip 1 CNV (unutar sub-RPE prostora, koji obično odgovara angiografski okultnom CNV-u), tip 2 CNV (unutar subretinalnog prostora, koji obično odgovara angiografski klasičnoj CNV) i tip 3 CNV (intraretinalna angiomatska proliferacija). Takvi krvni sudovi propuštaju tečnost (koja se može nakupljati ispod retinalnog pigmentnog epitela, subretinalno ili intraretinalno) i skloni su pucanju što narušava funkciju retine. Endotelni faktor rasta (VEGF) ključan je u patogenezi vlažne (eksudativne-neovasklurane) AMD, što potvrđuje jaka korelacija između nivoa VEGF-a u očnoj vodici i vitreusu, te stvaranju aktivnih krvnih sudova u neovaskularnim bolestima retine. Oštećenje retine usljed neovaskularizacije rezultuje teškim, progresivnim, ireverzibilnim oštećenjem vida.
Najčešći simptomi uključuju metamorfopsiju, skotome, fotopsiju te poteškoće u adaptaciji na tamu. Ukoliko je zahvaćeno samo jedno oko, simptomi mogu postati vidljivi tek kad se drugo, zdravo oko zatvori. Glavna odrednica oštećenja uzrokovanog lezijom horoidalne neovaskularizacije je dužina trajanja eksudativne bolesti. Bez liječenja, većina zahvaćenih očiju završava teškim oštećenjem centralnog vida (0.1) unutar 12 mjeseci, te sljepoćom što ima značajan uticaj na kvalitet života i samostalno funkcionisanje bolesnika. Bolesnici imaju veći nivo stresa, niže opšte zadovoljstvo, niži nivo tjelesne aktivnosti i povećanu učestalost depresije u odnosu na osobe iste dobi bez AMD-a. Zlatni standard u dijagnostici vlažnog oblika AMD je fluoresceinska angiografija. U praksi se vrlo često koristi optička koherentna tomografija (OCT) i OCT-angiografija koje omogućavaju slikoviti prikaz kojim se može detektovati subretinalna tečnost i centralna debljina retine.
Iako je AMD treći vodeći uzrok ireverzibilnog gubitka vida širom svijeta, incidencija teškog ireverzibilnog gubitka vida, pravno definisane sljepoće i oštećenja vidne funkcije znatno se smanjila s početkom liječenja AMD-a ljekovima koji djeluju na vaskularni endotelni faktor rasta (VEGF). Intravitrealna primjena anti-VEGF ljekova danas je standard liječenja. Anti-VEGF ljekovi inhibiraju signalizacijske puteve VEGF čime se zaustavlja razvoj neovaskularnih lezija, te rešava edem retine kod bolesnika s vlažnim oblikom AMD. Ranije uvođenje potentnijeg anti-VEGF lijeka dovodi do bržeg isušivanja retinalne tečnosti, boljih anatomskih i funkcionalnih ishoda i bolje prognoze bolesti. Dva lijeka trenutno odobrena za liječenje vlažnog oblika AMD dostupna su na tržištu: ranibizumab (Lucentis®) i aflibercept (Eylea®).
U Crnoj Gori, u Klinici za očne bolesti – KCCG terapija koja se primjenjuje za liječenje vlažnog oblika AMD jesu: ranibizumab (Lucentis®) i aflibercept (Eylea®). Međutim, kroz dugogodišnju kliničku praksu i praćenje retinoloških bolesnika, pokazalo se da određeni broj bolesnika liječenih ranibizumabom i afliberceptom ne postiže zadovoljavajuće rezultate, te isti završavaju praktično sljepoćom. Kod 25% svih bolesnika i uprkos liječenju intravitrealnim anti-VEGF injekcijama ne dolazi do poboljšanja i/ili održavanja vidne oštrine. Iz naše kliničke prakse taj broj se kreće od 15-20%. Klinička ispitivanja pokazala su da novi lijek brolucizumab (Beovu) u liječenju poremećaja vida uzrokovanog neovaskularnom AMD dovodi do značajno boljeg anatomskog ishoda i dovodi do poboljšanja najbolje korigirane vidne oštrine (BCVA) jednakog onome uz aflibercept. Mogućnost rjeđeg doziranja (svakih 12 nedjelja nakon udarne doze) smanjuje broj dolazaka u bolnicu, smanjuje broj injekcija čime se može povećati saradnja bolesnika, i iz tog razloga brolucizumab bi predstavljao novu opciju za efektivnije i sigurno liječenja bolesnika s vlažnim oblikom senilne makularne degeneracije.
Literatura:
- American Academy of Ophthalmology. Retina and vitreous, BCSC 12, San Francisco: American Academy of Ophthalmology, 2016-2017.
- Wong WL, Su X, Li X, et al. Global prevalence of age-related macular degeneration and disease burden projection for 2020 and 2040: a systematic review and meta-analysis. Lancet Glob Health. 2014;2(2):e106–16. doi:10.1016/S2214-109X(13)70145-1
- Laurence S Lim 1 , Paul Mitchell, Johanna M Seddon, Frank G Holz, Tien Y Wong, Age-related Macular Degeneration , Lancet 379 (9827), 1728-38 2012 May 5 DOI: 10.1016/S0140-6736(12)60282-7
- Kanski, J. and Bowling, B. (2016). Kanski's Clinical ophthalmology.Elsevier Limited
- Ratnapriya R, Chew EY. Age-related macular degeneration-clinical review and genetics update. Clin Genet. 2013:84(2):160-166
- AREDS2 Research Group, The Age-Related Eye Disease Study 2 (AREDS2): Study Design and Baseline Characteristics (AREDS2 Report Number 1), Ophthalmology 119 (11), 2282-9 Nov 2012, DOI: 10.1016/j.ophtha.2012.05.027
7. Fritsche LG, Fariss RN, Stambolian D, Abecasis GR, Curcio CA, Swaroop A. Age-related macular degeneration: genetics and biology coming together. Annu Rev Genomics Hum Genet 2014; 15: 151–71.
8. Fritsche LG, Igl W, Bailey JN, et al. A large genome-wide association study of age-related macular degeneration highlights contributions of rare and common variants. Nat Genet 2016; 48: 134–43.
- Spilsbury K, Garrett KL, Shen WY, et al. Overexpression of vascular endothelial growth factor (VEGF) in the retinal pigment epithelium leads to the development of choroidal neovascularization. Am J Pathol 2000;157:135–44
- Klein R, Klein BE, Linton KL. Prevalence of age-related maculopathy. The Beaver Dam Eye Study. Ophthalmology. 1992;99:933-943.
- Lucentis SmPC https://www.ema.europa.eu/en/documents/product-information/lucentis-epar-product-information_en.pdf
- Eylea SmPC https://www.ema.europa.eu/en/documents/product-information/eylea-epar-product-information_en.pdf
- Ferris FL 3rd, Wilkinson CP, Bird A, et al. Clinical classification of age-related macular degeneration. Ophthalmology 2013; 120: 844–51.
- Brody BL, Gamst AC, Williams RA, et al. Depression, visual acuity, comorbidity, and disability associated with age-related macular degeneration. Ophthalmology 2001; 108: 1893–901.
- H&H: Dugel PU, Koh A, Ogura Y, Jaffe GJ, Schmidt-Erfurth U, Brown DM, et al. HAWK and HARRIER: phase 3, multicenter, randomized, double-masked trials of brolucizumab for neovascular age-related macular degeneration. Ophthalmology 2020;127: 72–84. https://doi.org/10.1016/j.ophtha.2019.04.017
- Lim LS, Mitchell P, Seddon JM, Holz FG, Wong TY. Age-related macular degeneration. Lancet 2012; 379: 1728–38.
- Bourne RR, Stevens GA, White RA, et al. Causes of vision loss worldwide, 1990–2010: a systematic analysis. Lancet Glob Health 2013; 1: e339–49









Add comment