Trening „Edukacija novinara povodom predstojeće COVID-19 imunizacije“ u organizaciji Instituta za javno zdravlje (IJZ) bio je odlična prilika za Institut za ljekove i medicinska sredstva (CInMED) da predstavnicima crnogorskih medija, kao vrlo značajnim učesnicima u sistemu farmakovigilance predstavi način praćenja bezbjednosti primjene vakcina, s posebnim osvrtom na primjenu vakcina protiv COVID19.
Interpretacija, razumijevanje i komunikacija o podacima koji se odnose na bezbjednost primjene ljekova i vakcina je vrlo osjetljivo pitanje, ujedno i prostor za bližu saradnju CInMED i medija, a sve u cilju objektivne informisanosti naše stručne i opšte javnosti. U uslovima COVID19 pandemije, kada je na sceni dodatno prisutna i infodemija, saradnja dobija još više na značaju. Od samog početka pandemije, mediji, očekivano, predstavljaju zainteresovanu stranu, koja svakodnevno informiše građane o aktuelnim stvarima vezano za pandemiju COVID19. Edukacija medija o farmakovigilanci i drugim aspektima primjene ljekova i vakcina kroz adekvatno informisanje građana doprinosi očuvanju javnog i zdravlja pojedinca.
Na početku prezentacije Maja Stanković iz CInMED je istakla značaj farmakovigilanci u eri COVID19. Naime, značajan izazov u komunikaciji i interpretaciji podataka o farmakovigilanci vakcina leži u činjenici da su vakcine protiv COVID19 novi ljekovi, odnosno ljekovi u liječenju nove bolesti i da će se u kratkom vremenskom periodu sprovesti masovna imunizacija, tj. primjena velikog broja doza vakcina, na raznovrsnoj populaciji. Upravo zbog toga je bitno da stručna i opšta javnost, kao i naši mediji razumiju koncept farmakovigilance tj. potrebe kontinuiranog praćenja bezbjednosti ljekova i vakcina.
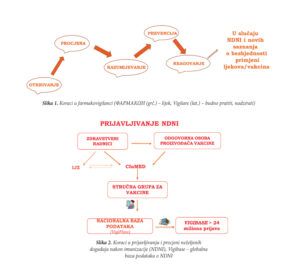
Predstavnici medija su upoznati sa ključnim koracima u procesu farmakovigilance, od otkrivanja neželjenih dejstava/događaja, preko njihove procjene, razumijevanja, prevencije i konačno reagovanja od strane nadležnih institucija, ukoliko se procijeni da je potrebno. Sve ove aktivnosti u farmakovigilanci prati komunikacija i vrlo je bitno da ona bude adekvatna.
 Predstavnici medija su upoznati i sa definicijom neželjenog događaja nakon imunizacije (NDNI), kao medicinskog događaja koji se ispoljio nakon imunizacije a koji ne mora biti nužno u vezi sa imunizacijom. Dalje, u prezentaciji je navedeno da su zahtjevi za registraciju i farmakovigilancu vakcina strožiji u odnosu na ostale ljekove tj. da vakcine predstavljaju izuzetno regulisane proizvode, uzimajući u obzir povećano interesovanje stručne i opšte javnosti kao i činjenicu da se vakcine najćešće primjenjuju preventivno, u zdravoj populaciji. Praćenje bezbjednosti vakcina je uključeno u sve faze razvoja vakcina, koje prethode njihovom stavljanju u promet. Dakle, i u pretkliničkoj fazi (ispitivanja na eksperimentalnim životinjama) i u svim fazama kliničkog razvoja vakcina. Nakon pozitivne procjene od strane nezavisnih tijela i eksperata svih faza ispitivanja koje je sproveo proizvođač, proces praćenja bezbjednosti vakcina i dalje traje, dokle god su prisutni na tržištu. Zapravo, makon registracije, ulazi se u ključnu fazu, tkz. postmarketinšku fazu praćenja bezbjednosti vakcina koja podrazumjeva potvrdu bezbjednosti njihove primjene na velikom broju ljudi, različitih zdravstvenih stanja. Dakle, iz kontrolisanih uslova koji karakterišu klinička ispitivanja prelazimo u “realni život” vakcina. Vrlo je bitno da svi u zdravstvenom sistemu, prvenstveno zdravstveni radnici budu budni u prepoznavanju i prijavljivanju nadležnim institucijama (CInMED i IJZ) neželjenih događaja nakon imunizacije.
Predstavnici medija su upoznati i sa definicijom neželjenog događaja nakon imunizacije (NDNI), kao medicinskog događaja koji se ispoljio nakon imunizacije a koji ne mora biti nužno u vezi sa imunizacijom. Dalje, u prezentaciji je navedeno da su zahtjevi za registraciju i farmakovigilancu vakcina strožiji u odnosu na ostale ljekove tj. da vakcine predstavljaju izuzetno regulisane proizvode, uzimajući u obzir povećano interesovanje stručne i opšte javnosti kao i činjenicu da se vakcine najćešće primjenjuju preventivno, u zdravoj populaciji. Praćenje bezbjednosti vakcina je uključeno u sve faze razvoja vakcina, koje prethode njihovom stavljanju u promet. Dakle, i u pretkliničkoj fazi (ispitivanja na eksperimentalnim životinjama) i u svim fazama kliničkog razvoja vakcina. Nakon pozitivne procjene od strane nezavisnih tijela i eksperata svih faza ispitivanja koje je sproveo proizvođač, proces praćenja bezbjednosti vakcina i dalje traje, dokle god su prisutni na tržištu. Zapravo, makon registracije, ulazi se u ključnu fazu, tkz. postmarketinšku fazu praćenja bezbjednosti vakcina koja podrazumjeva potvrdu bezbjednosti njihove primjene na velikom broju ljudi, različitih zdravstvenih stanja. Dakle, iz kontrolisanih uslova koji karakterišu klinička ispitivanja prelazimo u “realni život” vakcina. Vrlo je bitno da svi u zdravstvenom sistemu, prvenstveno zdravstveni radnici budu budni u prepoznavanju i prijavljivanju nadležnim institucijama (CInMED i IJZ) neželjenih događaja nakon imunizacije.
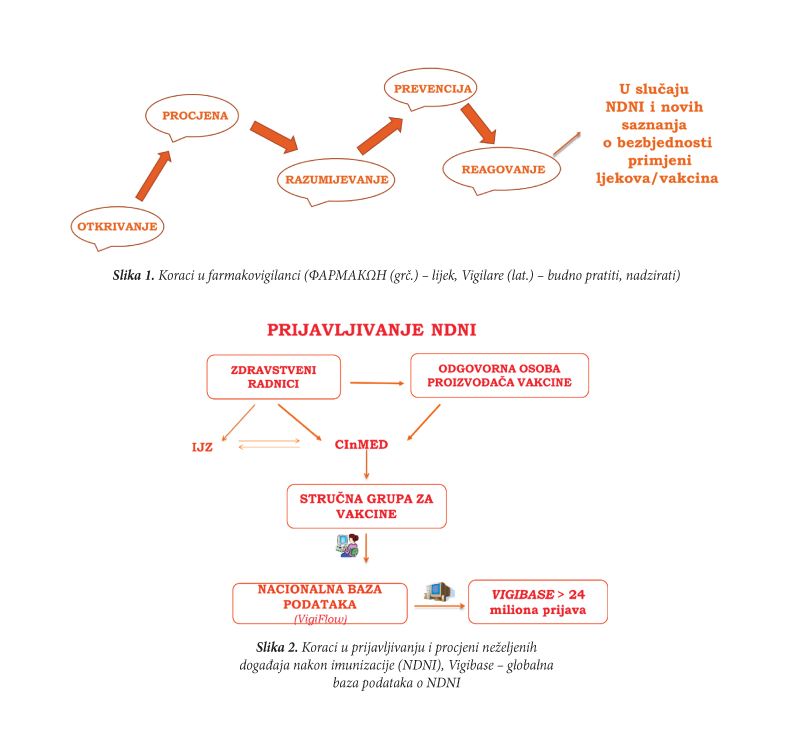
Sve prijavljene neželjene događaje, stručna grupa za vakcine koja uključuje predstavnike CInMED, IJZ i kliničare će procijeniti s aspekta očekivanosti, ozbiljnosti i uzročno posljedične povezanosti sa primijenjenom vakcinom. Svaka prijava neželjenog dejstva vakcine se unosi u nacionalnu bazu podataka o neželjenim dejstvima, kao i u globalnu bazu podataka, počev od 2009. godine, godine osnivanja Agencije za ljekove i medicinska sredstva (CALIMS) koja je preteča CInMED. Globalnu bazu podataka o neželjenim dejstvima svih ljekova, uključujuči i vakcina, vodi kolaborativni centar Svjetske zdravstvene organizacije – Upsala Monitoring Centar (UMC), a Program globalnog praćenja bezbjednosti se odvija pod pokroviteljstvom Svjetske zdravstvene organizacije.
Predstavnicima medija je od strane Maje Stanković dalje ukazano na transparentnost CInMED u izvještavanju o neželjenim događajima nakon imunizacije i uopšte primjene svih ljekova. CInMED objavljuje svake godine godišnji izvještaj o neželjenim dejstvima ljekova, koja su prijavljena CInMED u prethodnoj kalendarskoj godini. Sastavni dio ovog izvještaja je i analiza prijavljenih neželjenih događaja nakon primjene vakcina. U nastavku prezentacije Maja Stanković je prikazala statistiku iz lokalne baze podataka o neželjenim dejstvima vakcina za period od 2009-2020, kao i dosadašnju statistiku iz globalne baze podataka o bezbjednosti različitih vakcina protiv COVID19 koje se primjenjuju širom svijeta. Analiza dosadašnjih podataka o bezbjednosti primjene vakcina protiv COVID19 potvrđuje rezultate dobijene u kliničkim ispitivanjima, koja su prethodila njihovom stavljanju u promet. Najčešći neželjeni događaji koji se očekuje su lokalne reakcije na mjestu primjene vakcina, koje su uglavnom blage i umjerene po intenzitetu i najčešće prolaze spontano, bez potrebe za medicinskom terapijom.
Predstavnici medija su dalje informisani o tome da je CInMED u saradni sa IJZ, razvio za zdravstvene radnike veliki broj mogućnosti za prijavljivanje neželjenih događaja nakon imunizacije, kako bi proces prijavljivanja bio što jednostavniji. Od obrasca za prijavljivanje koji je dostupan na CInMED portalu, preko online forme za prijavu kojoj se takođe pristupa preko portala CInMED do preporučenog načina prijavljivanja putem informacionog sistema koji naši zdravstveni radnici koriste u svakodnevnom radu. Ovaj način prijavljivanja je omogućen izabranim doktorima za odrasle i ljekarima u opštim bolnicama.
Predstavnici medija su informisani o dokumentima Sažetak karakteristika lijeka i Uputstvo za pacijenta jedne od vakcina koja je odobrena za primjenu u zemljama Evropske unije. U pitanju su dokumenta koja su namijenjena zdravstvenim radnicima i pacijentima, kao relevantan izvor informacija o kvalitetu, bezbjednosti i efikasnosti vakcina protiv COVID19.
Maja Stanković je dalje tokom prezentacije naglasila da su podaci o bezbjednosti za vakcine protiv COVID19, koje se trenutno primjenjuju u svijetu, potvrdili da korist od njihove primjene višestruko prevazilazi rizik od ispoljavanja neželjenih događaja. Najbolja potvrda njihove bezbjednosti leži u činjenici da uprkos masovnoj imunizaciji i većoj mogućnosti ispoljavanja koincidentalnih događaja koji se mogu bez razloga pripisati primijenjenoj vakcini, vakcinacija protiv COVID19 u svijetu nesmetano teče tj nigdje nije privremeno obustavljena iz razloga problema sa bezbjednošću vakcine.
U zaključku predstavnici medija su informisani o tome da brz razvoj vakcina protiv COVID19 nije značio i manje standarde vezano za NJIHOV kvalitet, efikasnost i bezbjednost, da je veliki broj ljudi učestvovao u kliničkim ispitivanjima, značajno veči od standarda koje zahtijevaju principi dobre kliničke prakse, da je veliki broj vakcina razvijen u saradnji proizvođača sa renomiranim univerzitetima, te da je većina neželjenih dejstava prijavljenih do sada očekivana i prolazna.
Na kraju je istaknuto da je potrebno aktivno učešće svih u sistemu zdravstva, u cilju optimizacije nadzora nad neželjenim događajima nakon imunizaicije kao i da je doprinos medija u ovom procesu od vitalnog značaja.
Maja Stanković
Institut za ljekove i medicinska sredstva, CInMED







Add comment