Na osnovu Zakona o ljekovima (“Sl. list CG” br. 56/11 i “Sl. list CG” br. 06/13) i Pravilnika o načinu prikupljanja podataka i načinu prijavljivanja i praćenja neželjenih dejstava ljekova za upotrebu u humanoj medicini (“Sl. list CG” br. 46/14) Agencija za ljekove i medicinska sredstva Crne Gore (CALIMS) je nadležna za praćenje neželjenih dejstava, odnosno bezbjednosti ljekova i detekcije svake promjene u odnosu koristi i rizika njihove primjene.
Prijavljivanje neželjenih dejstava ljekova ima važnu ulogu u dobijanju novih informacija o ljekovima koji su već u prometu (nova neželjena dejstva, posebna upozorenja i mjere opreza, kontraindikacije i sl.). CALIMS prikuplja, obrađuje i analizira neželjena dejstva ljekova koja su prijavljena od strane zdravstvenih radnika i odgovornih lica za farmakovigilancu u farmaceutskim kompanijama i ista prosljeđuje u svjetsku bazu podataka za praćenje neželjenih dejstava, koju održava kolaborativni centar Svjetske zdravstvene organizacije (WHO – World Health Organization) koji se nalazi u Upsali (Švedska). Na osnovu prikupljenih informacija CALIMS, u cilju očuvanja javnog zdravlja, može donijeti određene regulatorne mjere koje su definisane Zakonom o ljekovima.
CALIMS svake godine objavljuje detaljan izvještaj o rezultatima prijavljenih neželjenih dejstava ljekova, koja su se ispoljila na teritoriji Crne Gore. Izvještaj za 2015. godinu je šesti godišnji izvještaj, urađen od strane Odjeljenja za farmakovigilancu CALIMS, i odnosi se na prijave primljene i obrađene u periodu od 01.01.2015. do 31.12.2015. Godišnji izvještaj sadrži i kratak pregled najznačajnijih bezbjednosnih regulatornih mjera, koje je CALIMS donijela na osnovu novih saznanja o odnosu korist/rizik od primjene određenih ljekova, nakon odluke nadležnih evropskih tijela u oblasti ljekova.
Izvještaj za 2015. godinu, kao i izvještaji za prethodne godine su dostupni na portalu CALIMS (www.calims.me).
U prethodnom broju časopisa Medical CG (broj 85, 05. maj 2016.) prikazan je prvi dio odabranih poglavlja izvještaja koja se odnose na izvore prijava, profil primarnog izvještača, izvore prijava prema zdravstvenim ustanovama i izvore prijava prema farmaceutskim kompanijama.
U nastavku teksta, dat je osvrt na analizu prijava u odnosu na anatomsko-terapijsko-hemijsku (ATC) klasifikaciju suspektnog lijeka, kao i klasifikaciju neželjenih dejstava prema sistemima organa na kojima se ispoljavaju.
Analiza prijava u odnosu na anatomsko-terapijsko-hemijsku (ATC) klasifikaciju suspektnog lijeka
Potrebno je istaći da jedna prijava može da sadrži više neželjenih reakcija, kao i ljekova za koje se sumnja da su doveli do njihovog ispoljavanja. Tako je ukupan broj prijavljenih pojedinačnih neželjenih reakcija, odnosno ljekova pod sumnjom, veći od ukupnog broja prijava.
U ukupno 132 prikupljenih prijava, 138 ljekova je označeno kao suspektan lijek. Najveći broj prijava se, prema ATC klasifikaciji suspektnih ljekova, odnosio na ljekove koji pripadaju grupi ljekova koji djeluju na kardiovaskularni sistem (grupa C), antiinfektivnim ljekovima za sistemsku primjenu (grupa J), kao i antineoplasticima i imunomodulatorima (grupa L) (Slika 1.).

Klasifikacija neželjenih dejstava prema sistemima organa na kojima se ispoljavaju
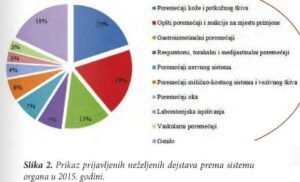
Kako je moguće da se kod jednog pacijenta istovremeno ispolji više neželjenih dejstava određenog lijeka, broj neželjenih dejstava opisanih u prijavama je znatno veći od broja primljenih prijava. U vremenskom periodu koji je obuhvaćen ovim izvještajem, ukupno je prijavljeno 317 neželjenih reakcija, od kojih najveći broj čine: poremećaji kože i potkožnog tkiva (20%), opšti poremećaji i reakcije na mjestu primjene (19%), gastrointestinalni poremećaji (13%), respiratorni, torakalni i medijastinalni poremećaji (7%), poremećaji nervnog sistema (7%) i poremećaji mišićno-kostnog sistema i vezivnog tkiva (6%) (Slika 2.)
U tabeli 1 dat je prikaz najčešće prijavljivanih neželjenih dejstava tokom 2015. godine. Najčešće prijavljivana neželjena dejstva uglavnom nijesu ozbiljnog karaktera i očekivana su nakon primjene suspektnih ljekova.
|
NEŽELJENO DEJSTVO |
BROJ PRIJAVA |
|
raš |
22 (7%) |
|
reakcije na mjestu primjene |
21 (7%) |
|
eritem |
14 (4%) |
|
mučnina |
13 (4%) |
|
kašalj |
12 (4%) |
|
svrab |
10 (3%) |
|
glavobolja |
9 (3%) |
|
urtikarija |
6 (2%) |
|
periferni edem |
6 (2%) |
|
abdominalni bol |
6 (2%) |











Add comment