Dr Rifat Međedović
Klinički centar Crne Gore
Psorijazni artritis
Psorijazni artritis (PsA) je hronični artritis, klinički heterogen i povezan sa psorijazom (PsO). Osim zahvatanja zglobova, PsA se karakteriše i zahvatanjem perizglobnih struktura, tetivnih pripoja za kost (entezitis), tenosinovitisom cijelih prstiju (daktilitis), ili može uzrokovati promjene na noktima (kao što su pitting i oniholiza). Osim pomenutog, kod PsA može doći do inflamacije u regiji sakroilijačnih zglobova i kičmenog stuba (sakroileitis, spondilitis). Prevalencija PsA u opštoj populaciji varira od 0.1% do 1%, sa većom prevalencijom od 6% do 42% kod bolesnika sa PsO, a najčešće se javlja u dobi od 30 do 50 godina i gotovo podjednako u oba pola. Genetska predispozicija ima ulogu u nastanku PsA, što se ogleda u povezanosti sa HLA antigenima (HLA B27 i B39), kao i u jasnoj porodičnoj predispoziciji pojavljivanja ove bolesti. Do 40% bolesnika sa PsA ima pozitivnu porodičnu anamnezu o PsO ili PsA. Najvažniji faktor rizika za PsA je PsO, i u studijama se navodi da 5% do 30% osoba sa PsO oboli od PsA, najčešće oko 25%. Kod većine bolesnika se prvo javljaju kožne promjene, a potom zahvatanje zglobova, perizglobnih struktura ili kičmenog stuba, dok se kod oko 10% bolesnika promjene javljaju istovremeno, a kod oko 10% bolesnika zglobne promjene se čak mogu pojaviti i prije kožnih (psorijazni artritis bez psorijaze). U samoj patogenezi bolesti najvažniji faktori su: genetska predispozicija, faktori spoljne sredine i imunološki. Nije do kraja i precizno definisan imunološki slijed dešavanja u nastanku PsO i PsA i njihovih manifestacija, ali se zna da dolazi do dominantno aktivacije T ćelijskog imunskog odgovora, Th17 odgovora i da su ključni citokini i kada je riječ o inflamaciji i kada je riječ o oštećenju TNF alfa (tumor necrosis factor alfa), IL17 (interleukin 17) i IL23 (IL12/IL23 citokinski put). Bilo da je riječ o zglobu, tetivi, entezalnom pripoju, ili aksijalnom skeletu, bolest se ispoljava bolom, bolnom osjetljivošću, otokom i ograničenom i bolnom pokretljivošću. Bolest se može ispoljiti monoartikularnim, oligoartikularnim ili poliartikularnim oblikom, ali i spondilitisnim. Najčešće zahvata koljena, skočne zglobove i male zglobove stopala, dok je najčešća lokalizacija entezitisa u regiji pripoja Ahilove tetive i plantarne fascije za petnu kost. Sistemske manifestacije bolesti su u vidu slabosti, malaksalosti, nekada promjenama na očima (uveitis), čak i aorti (aortitis), crijevima (kolitis), srcu (srčana slabost) i plućima (pleuritis, pneumonitis). Dijagnoza PsA se postavlja na osnovu kliničkih manifestacija bolesti, a zbog velike kliničke heterogenosti ASAS (Assessment of SpondyloArthritis International Society) grupa i CASPAR (Classiffication of Psoriatic arthritis) grupa su predložili klasifikacione kriterijume za postavljanje dijagnoze PsA. I jedni i drugi podrazumijevaju postojanje PsO u ličnoj ili porodičnoj istoriji bolesti.
Psorijaza i psorijazni artritis – sistemska bolest
I PsO i PsA predstavljaju sistemske i imunoposredovane bolesti, sa dokazanom ulogom proinflamatornih citokina. Njihova sistemska priroda se ne ogleda samo u sistemskim simptomima (slabost, malaksalost, isrpljenost) i u patogenezi bolesti koja je proinflamatorno imunoposredovana (TNF alfa, IL17, IL23), već i u povećanom riziku od komorbiditeta od kojih su najznačajniji: kardiovaskularne bolesti, šećerna bolest, gojaznost, inflamatorna bolest crijeva, nealkoholni steatohepatitis i dr. Studije su i pokazale jasno povećan rizik u poređenju sa opštom populacijom. U literaturi se akcentuje sistemsko porijeklo bolesti čak i kod izolovane PsO, i bez PsA, a sve se češće uvodi termin „psorijazna bolest“. Znajući da se PsO javlja kod 1-3% opšte populacije, a PsA kod 0.1- 1% opšte populacije, problem dobija na značaju. Povećana koncentracija proinflamatornih citokina se nalazi u kožnim lezijama, zglobovima i perizglobnim strukturama (tetive, enteze, sakroilijačni zglobovi, kičmeni stub), ali i u cirkulaciji. Čak su studije pokazale, njihovu povećanu koncentraciju kod bolesnika sa PsO koji su asimptomatski i nemaju manifestacije PsA. Takođe, njihova povećana koncentracija u cirkulaciji dokazana je kod bolesnika sa PsO kod kojih još uvijek nije potvrđeno postojanje nekih od komorbiditeta (metabolički sindrom, hipertenzija i dr). U velikom procentu bolesnici sa PsO a posebno sa PsA imaju subklinički dokazanu inflamaciju i u potkožnom tkivu, zglobovima, entezalnim pripojima, zidu krvnih sudova (kao što su aorta i njene grane), zidu crijeva, plućnom parenhimu itd. Sve je to potkrijepljeno i činjenicom da je dokazano da predloženi sistemski ljekovi za liječenje PsO (kod umjerenih i težih formi bolesti) i bolest modifikujući ljekovi (BML) za liječenje PsA (kod blagih, umjerenih i teških formi bolesti), osim što djeluju na same kliničke manifestacije ovih bolesti, itekako imaju efekta i na sistemske manifestacije. A ono što je još važnije smanjuju produkciju ključnih proinflamatornih citokina, redukuju sistemsku inflamaciju i njen stalni i perzistentni stimulus aterogeneze, trombogeneze, potencijalnih trombotičkih kardiovaskularnih događaja, kao i insulinske rezistencije, poremećaja glikoregulacije i lipidogeneze.
Liječenje psorijaznog artritisa – posebni klinički domeni bolesti (entezitis, daktilitis, aksijalna bolest, komorbiditeti)
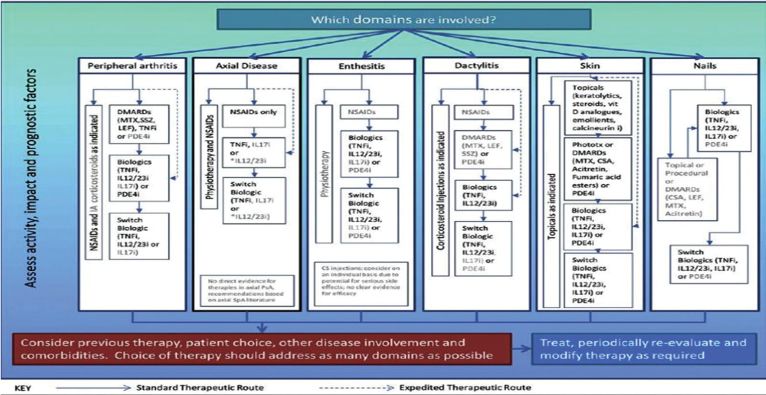
Noviji podaci i otkrića na pomenutu temu su doprinijeli da se i pristup u liječenju PsO i PsA promijeni. Raniji terapijski ciljevi su bili: ublažavanje simptoma, smanjenje inflamacije u regiji zahvaćene kože, zgloba ili dr strukture, sprečavanje nastanka ireverzibilnih oštećenja, i time poboljšanje kvaliteta života bolesnika i funkcionalnog statusa. Sada se nameće potreba za suzbijanjenm sistemske inflamacije koja je prisutna i kod bolesnika sa PsO i PsA, a takođe i suzbijanje subkliničke inflamacije krvnih sudova i pojedinih organa, koja svakako predstavlja predispoziciju i snažan faktor rizika za buduće kliničko ispoljavanje. U oblasti dermatologije se nazivaju sistemskim ljekovima, u oblasti reumatologije nazivaju BML, i oni imaju osobinu da djeluju i na sami patofiziološkim mehanizam bolesti, čime smanjuju produkciju proinflamatornih citokina čime se smanjuje inflamacija kako u regiji ciljnih organa tako i sistemski. Time se postiže i smanjuje i efekat sistemskih manifestacija bolesti kod PsO i PsA, redukuju metabolički, kardiovaskularni i drugi rizici. EULAR (European Leage Against Rheumatism) preporuke i GRAPPA (Group for Research and Assessment of Psoriasis and Psoriatic arthritis) preporuke za liječenje PsA se zasnivaju na kliničkim manifestacijama bolesti (kožnim, zglobnim, sistemskim). GRAPPA preporuke iz 2018.godine su prikazane na slici.
 Obzirom da se radi o hroničnoj i neizlječivoj bolesti, u samom liječenju definisana je strategija „treat to target“ („liječenjem do cilja“) koja je kako u kliničkim studijama tako i u kliničkoj praksi dala odlične rezultate. Ona se zasniva na ranoj dijagnozi bolesti i ranom agresivnom tretmanu iste (ranom započinjanju liječenja specifičnim BML), uz intezivno praćenje bolesnika kako bi dalji terapijski modalitet bio nastavljen ili promijenjen u slučaju potrebe. Najveći broj BML koji se koriste u liječenju PsA pokazali su odličan efekat i na kožne i na zglobne manifestacije bolesti. Oni iz grupe bioloških ljekova, kao i malih molekula (JAK inhibitora), takođe imaju odličan terapijskih efekat i na aksijalnu prezentaciju bolesti, entezitise i daktilitise. U grupi konvencionalnih sintetskih BML (ksBML) kroz kliničke studije najveću efikasnost pokazao je metotreksat, pa se i u samim preporukama smatra lijekom prvog izbora. Osim njega, predloženi su sulfasalazin, leflunomid, dok se azatioprin i ciklosporin A manje koriste. Kada je u pitanju aksijalna bolest, a takođe i entezitisi i daktilitisi, dominantnu efikasnost su pokazali biološki BML (bBML) i ljekovi iz grupe malih molekula (inhibitori JAK kinaze). Ljekovi sa najviše kliničkog iskustva su anti TNF ljekovi (Infliksimab, Adalimumab, Golimumab, Etanercept i dr), ljekovi koji djeluju na ključne citokine (anti IL17 A – Sekukinumab, anti IL12/23 – Ustekinumab, i dr), kao i mali molekuli (JAK inhibitori – Tofacitinib i dr). Važno je reći da kod blažih formi bolesti, svoju ulogu u liječenju PsA imaju NSAIL (nesteroidni antiinflamatorni ljekovi) i glukokortikoidi, mada su glukokortikoidi mnogo efikasniji kada je u pitanju njihova lokalna primjena (intraartikularno, u samu entezu ili ovojnicu tetive), nego li sistemski. Važno je reći sa su bBML u odnosu na ksBML, pokazali podjednaku efikasnost i u regiji kože i zglobova, ali svakako veću efikasnost u regiji perizglobnih struktura, sakroilijačnih zglobova i kičmenog stuba, gdje je efekat konvencionalnih sintetskih BML ipak limitiran. Takođe, biološki ljekovi su se pokazali efikasnim i u slučajevima izostanka efekta konvencionalnih sintetskih BML, a to nije mali procenat bolesnika. Primjena sistemskih odnosno BML kod blažih formi bolesti može djelovati i preventivno, i spriječiti nastanak ozbiljnih kožnih i zglobih oštećenja, i komorbiditeta. U savremenim dermatološkim i reumatološkim smjernicama za liječenje PsO i PsA ostala je samo blaga forma PsO kod koje se preporučuju topijski preparati, za sve ostale forme PsO i PsA obavezna je primjena sistemskih i BML.
Obzirom da se radi o hroničnoj i neizlječivoj bolesti, u samom liječenju definisana je strategija „treat to target“ („liječenjem do cilja“) koja je kako u kliničkim studijama tako i u kliničkoj praksi dala odlične rezultate. Ona se zasniva na ranoj dijagnozi bolesti i ranom agresivnom tretmanu iste (ranom započinjanju liječenja specifičnim BML), uz intezivno praćenje bolesnika kako bi dalji terapijski modalitet bio nastavljen ili promijenjen u slučaju potrebe. Najveći broj BML koji se koriste u liječenju PsA pokazali su odličan efekat i na kožne i na zglobne manifestacije bolesti. Oni iz grupe bioloških ljekova, kao i malih molekula (JAK inhibitora), takođe imaju odličan terapijskih efekat i na aksijalnu prezentaciju bolesti, entezitise i daktilitise. U grupi konvencionalnih sintetskih BML (ksBML) kroz kliničke studije najveću efikasnost pokazao je metotreksat, pa se i u samim preporukama smatra lijekom prvog izbora. Osim njega, predloženi su sulfasalazin, leflunomid, dok se azatioprin i ciklosporin A manje koriste. Kada je u pitanju aksijalna bolest, a takođe i entezitisi i daktilitisi, dominantnu efikasnost su pokazali biološki BML (bBML) i ljekovi iz grupe malih molekula (inhibitori JAK kinaze). Ljekovi sa najviše kliničkog iskustva su anti TNF ljekovi (Infliksimab, Adalimumab, Golimumab, Etanercept i dr), ljekovi koji djeluju na ključne citokine (anti IL17 A – Sekukinumab, anti IL12/23 – Ustekinumab, i dr), kao i mali molekuli (JAK inhibitori – Tofacitinib i dr). Važno je reći da kod blažih formi bolesti, svoju ulogu u liječenju PsA imaju NSAIL (nesteroidni antiinflamatorni ljekovi) i glukokortikoidi, mada su glukokortikoidi mnogo efikasniji kada je u pitanju njihova lokalna primjena (intraartikularno, u samu entezu ili ovojnicu tetive), nego li sistemski. Važno je reći sa su bBML u odnosu na ksBML, pokazali podjednaku efikasnost i u regiji kože i zglobova, ali svakako veću efikasnost u regiji perizglobnih struktura, sakroilijačnih zglobova i kičmenog stuba, gdje je efekat konvencionalnih sintetskih BML ipak limitiran. Takođe, biološki ljekovi su se pokazali efikasnim i u slučajevima izostanka efekta konvencionalnih sintetskih BML, a to nije mali procenat bolesnika. Primjena sistemskih odnosno BML kod blažih formi bolesti može djelovati i preventivno, i spriječiti nastanak ozbiljnih kožnih i zglobih oštećenja, i komorbiditeta. U savremenim dermatološkim i reumatološkim smjernicama za liječenje PsO i PsA ostala je samo blaga forma PsO kod koje se preporučuju topijski preparati, za sve ostale forme PsO i PsA obavezna je primjena sistemskih i BML.









Add comment